药品概述
体外研究
AZD5991是有效的Mcl-1抑制剂,具有高选择性。AZD5991可与Mcl-1直接结合,通过激活依赖于Bak的线粒体凋亡途径快速诱导癌细胞凋亡,对骨髓瘤和急性髓系白血病效果尤为显著(GI50 < 100nM)。在一系列血液肿瘤和实体瘤来源的细胞系中,AZD5991有倾向性地杀死血液细胞。
体内研究
在几种多发性骨髓瘤和急性髓性白血病模型中,无论是单次耐受剂量给药或是与bortezomib/venetoclax组合给药,AZD5991都具有有效的抗肿瘤活性,能引起完全的肿瘤消退。在这些体内试验中,AZD5991的细胞毒性活性与其诱导线粒体凋亡途径相关。
在物理化学中,熵增原理告诉我们,分子是爱“自由”的,喜欢无序状态,不愿意被束缚(熵下降不是自发过程)。但是在药物化学中,药物分子拥有太多的自由旋转键是不利于与靶点的结合和口服吸收的(请参考Lipinski Ro5)。因为诱导契合假说告诉我们,分子与受体蛋白结合是动态过程,两者相互改变构象而适应彼此。可以想象适当的限制构象,将有利于减少这种匹配过程带来的熵损失,产生最佳的亲和力。因此,构象限制策略在先导化合物优化中是常常用到的手段。近日,阿斯利康科学家就利用这种策略开发出Mcl-1选择性抑制剂AZD5991,显示出对多种肿瘤很强的抑制活性,结果发表在Nature Communications 上。
Mcl-1属于抗凋亡蛋白Bcl-2家族成员,是细胞凋亡重要途径之一——线粒体凋亡途径的主要物质。Mcl-1基因在多种人类肿瘤中扩增,高表达的Mcl-1与化疗及靶向药物耐药性产生和疾病复发有密切关系。[1] 在肿瘤细胞内,Mcl-1与促凋亡蛋白(如Bak、Bid、Bad等)通过蛋白-蛋白相互作用(PPI)发挥抗凋亡作用,导致肿瘤细胞增殖。但这种PPI接触界面很大且亲和力强,对开发小分子药物产生较大困难,因此目前还没有Mcl-1抑制剂上市。阿斯利康的科学家通过解析小分子-蛋白共晶结构发现,化合物1(Kd< 5 μM)与Mcl-1存在2:1的比例,两个分子在活性位点相互靠近(两苯甲基相距3.5 Å)共同占据活性位点,同时羧基与Arg263形成离子键。[2] 考虑到1的溶解度差以及PPI界面很大,研究人员尝试合成二聚体3来提高作用力,发现Mcl-1的半抑制浓度(IC50)有巨大改进,达0.77 µM。更有意思的是,作为化合物3的副产物4,表现出更高的活性(IC50= 0.042 μM)。共晶结构显示其占据更大的疏水空间,并且采取“U”型构象,吡唑甲基与萘环仅相距3.6 Å(大概一个氢键距离,这点对后来结构修饰很重要)。

Mcl-1选择性抑制剂及共晶结构。图片来源:Nat. Commun.
基于化合物4与Mcl-1的共晶结构的特点,研究人员很容易想到将吡唑甲基同萘环通过linker连接起来限制构象或许能提高活性。这样大环化合物5应运而生,不出所料,大环化合物5对Mcl-1的活性远高于化合物4,IC50达到19 nM。进一步优化得到的氯代化合物7(光学异构体Ra-7,即AZD5991)对Mcl-1表现出最强的抑制活性(IC50 = 0.7 nM)和选择性(Bcl-2 IC50 = 20 µM、Bcl-xL IC50 = 36 µM、Bcl-w IC50 = 49 µM、Bfl-1 IC50 = 24µM)。

大环化合物表现出更高的活性和选择性。图片来源:Nat. Commun.
AZD5991对多种肿瘤细胞系有较强的抑制,尤其是血液肿瘤中急性髓细胞白血病(AML)、多发性骨髓瘤(MM)和非霍奇金淋巴瘤(NHL)。通过对多发性骨髓瘤细胞系MOLP-8 进行研究发现AZD5991通过增加线粒体外面渗透性(MOMP),激活caspase-3/7和磷脂酰丝氨酸外翻诱发细胞膜通透性增加及细胞ATP泄露进而导致细胞凋亡。

AZD5991引发的细胞凋亡机制以及对肿瘤细胞系的增殖抑制。图片来源:Nat. Commun.
在体内药效方面,AZD5991对小鼠多发性骨髓瘤模型(MOLP-8)和急性髓细胞白血病模型(MV4-11)表现出剂量依赖性抑制,当给药100 mg/kg时,两种肿瘤生长完全被抑制(TGI = 100%)!同时,在中剂量时(30 mg/kg或60 mg/kg)与蛋白酶体抑制剂bortezomib或Bcl-2抑制剂venetoclax也有很好的联用效果。所有模型中,在给药期间动物体重变化在可接受范围内,显示出初步的安全性。
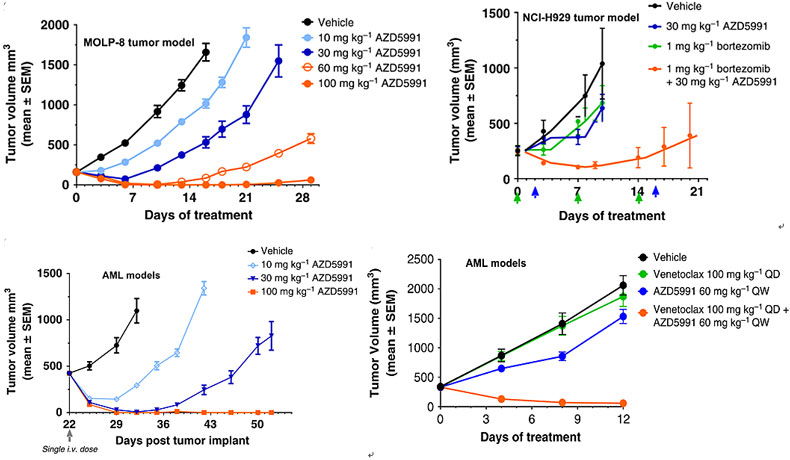
AZD5991对两种MM和AML模型的药效
——总结——
被缚的普罗米修斯给了人类更大的生存繁衍机会,而构象限制策略给了人类发现新药物甚至战胜疾病的道路。目前,AZD5991正处于临床1期,如果安全性和初步药效被证明,无疑给蛋白-蛋白相互作用小分子药物研发开启了一扇窗。

 京公网安备
11010802036025号
京公网安备
11010802036025号